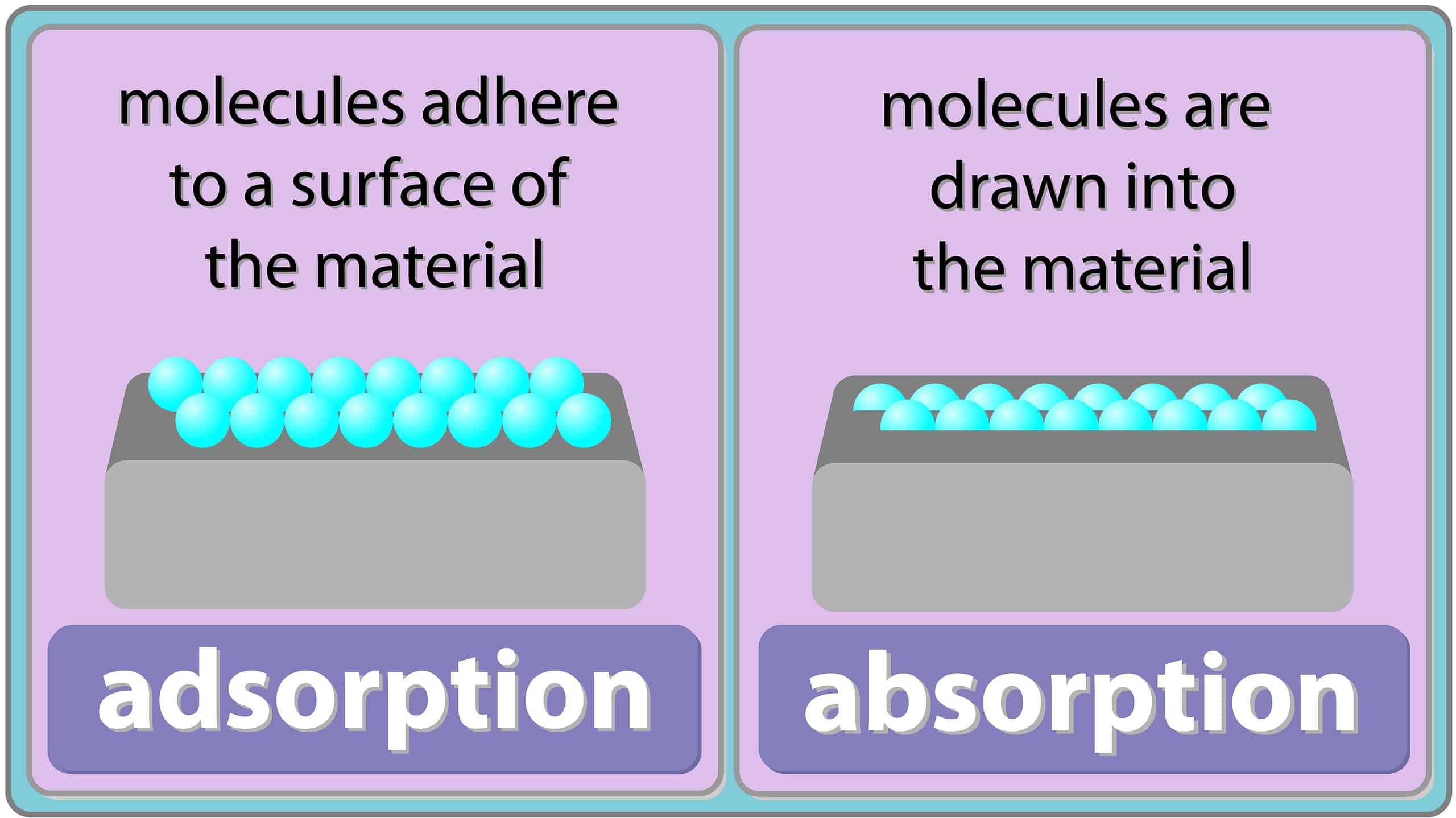
Ci sono molte differenze tra assorbimento e adsorbimento. Ad esempio, durante l’assorbimento, ioni, molecole e atomi entrano in una fase di massa, solida o liquida. Mentre il processo di adsorbimento si verifica quando solidi, gas o liquidi disciolti si attaccano o aderiscono liberamente alle superfici di altre sostanze, liquide o solide. Continua a leggere sull’assorbimento rispetto all’adsorbimento per conoscere le loro altre differenze.
Differenza primaria tra adsorbimento vs. Assorbimento
Una cosa che l’adsorbimento e l’assorbimento hanno in comune è che sono processi di assorbimento. Questo si riferisce a un processo chimico o fisico in cui una sostanza si collega a un’altra. Tuttavia ci sono molte differenze tra questi due processi, ma la loro differenza principale è la loro forza motrice. Ad esempio, la forza motrice dell’adsorbimento sono le forze insature sulla superficie solida, che si lega a un adsorbato. Pertanto, queste forze sono generalmente elettrostatiche o reversibili. Tuttavia, potenti interazioni comportano un trasferimento di elettroni ininterrotto tra il sorbente e il sorbato, che è irreversibile. Il motore dell’assorbimento è invece la differenza di concentrazione tra due fasi distinte.
Altre differenze tra adsorbimento e assorbimento
| Adsorbimento | Assorbimento |
|---|---|
| La definizione di adsorbimento è un’aggregazione di molecole, ioni o atomi sulla superficie dei materiali invece che alla rinfusa, principalmente liquidi o solidi. | La definizione di assorbimento è l’aggregazione di solidi, liquidi o gas disciolti attraverso la maggior parte del materiale, principalmente gas e liquidi |
| L’adsorbente ha spazi vuoti che stimolano l’adesione delle particelle sulla superficie | L’assorbimento avviene a causa della disponibilità di spazi molecolari e della natura delle particelle |
| Fenomeno di superficie | Fenomeno di massa |
| Il materiale adsorbito rimane attaccato all’adsorbente con legami covalenti o forze di Van der Wall. | Il materiale assorbito rimane nell’assorbente senza alcuna interazione chimica con l’assorbente. |
| Processo esotermico | Processo endotermico |
| Questo processo dipende dalla temperatura. Ad esempio, la bassa temperatura favorisce l’adsorbimento. | L’assorbimento non è influenzato dalla temperatura |
| L’adsorbato è più condensato sulla superficie rispetto alle altre parti dell’adsorbente dopo l’adsorbimento | La condensazione dell’assorbente nell’assorbente è uniforme dopo l’assorbimento |
| L’assorbimento aumenta costantemente e alla fine raggiunge l’equilibrio | L’assorbimento avviene in modo uniforme |
| L’adsorbato può essere separato facendo passare una nuova sostanza attraverso la superficie del materiale adsorbente, che sostituisce il precedente adsorbente. | L’assorbito può essere suddiviso in diverse fasi in base alla sua interazione chimica con le fasi. |
| Gli esempi includono analisi cromatografiche, segni di gas e purificazione dell’acqua. | Gli esempi includono la produzione di ghiaccio e la conservazione a freddo |
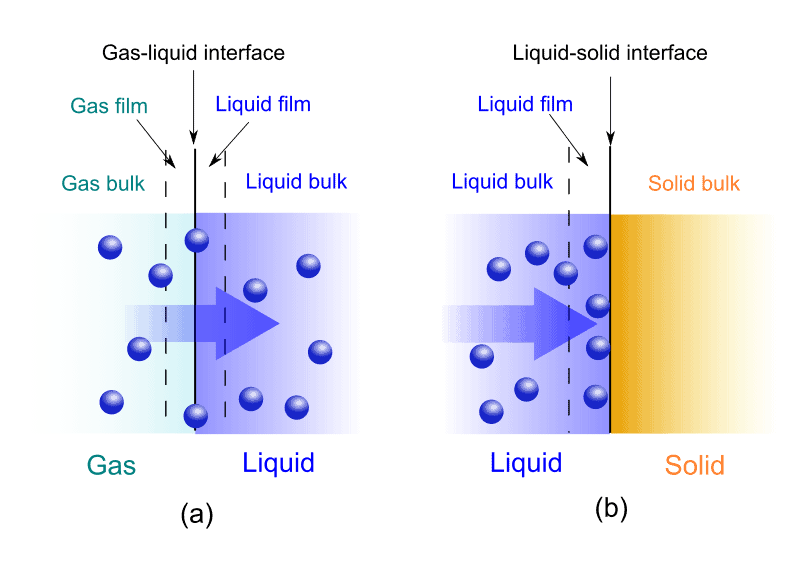
©Daniele Pugliesi / CC BY-SA 3.0b – License
Articoli correlati
Assorbimento: come funziona?
Questo processo comporta il trasferimento di massa di particelle attraverso la fase di massa di un’altra sostanza. Inoltre, il materiale che viene assorbito si chiama assorbente, mentre il materiale che assorbe si chiama assorbente.
Tipi di assorbimento
A seconda della natura dell’interazione tra assorbente e assorbente (chimica e fisica), esistono due tipi di assorbimento.
Assorbimento Chimico
Questo tipo di assorbimento comporta la reazione chimica tra l’assorbente e l’assorbente. Questo processo è utile per purificare le miscele chimiche e impedire che componenti indesiderati penetrino nel prodotto finale. Ad esempio, la rimozione del gas acido da parte dell’industria petrolifera. Inoltre, quando il gas naturale passa attraverso una soluzione acquosa di etanolamina, viene purificato. Tuttavia, l’etanolamina viene tipicamente utilizzata come scrubber per illuminare gli inquinanti acidi dai flussi di gas di scarico (come CO2 e H2S) mediante assorbimento chimico.
Assorbimento fisico
Questo tipo di assorbimento comporta un trasferimento di massa gas-liquido, che avviene al confine di fase. L’assorbimento fisico dipende da proprietà fisiche come pressione, solubilità e temperatura. Inoltre, è un processo non reattivo. Ad esempio, quando l’ossigeno nell’aria si dissolve in H2O.
Adsorbimento: come funziona?
Questo processo comporta l’adesione delle particelle esclusivamente sulla superficie di una sostanza. Il nome corretto per le sostanze assorbite è adsorbato, mentre la sostanza assorbita è nota come adsorbente.
Fisisorbimento (adsorbimento fisico)
Le deboli forze intermolecolari trattengono le molecole di adsorbato sulla superficie dell’adsorbente. Il fisisorbimento è considerato un processo reversibile a causa del suo debole legame dovuto alle interazioni di Van der Waals e in genere durante questo processo si verifica una formazione multistrato. Inoltre, è caratterizzato dalla bassa entalpia dell’adsorbimento.
Chemisorbimento (adsorbimento chimico)
Questo tipo di adsorbimento è di natura altamente specifica e si verifica solo quando esiste un legame chimico tra adsorbato e adsorbente. A differenza del fisisorbimento, l’unica formazione che si verifica è un monostrato. Inoltre, il chemisorbimento è irreversibile a causa delle sue forti forze motrici ed è caratterizzato dall’elevata entalpia dell’adsorbimento.
Esempi di assorbimento
Questo processo si verifica quando molecole, ioni e atomi passano in un materiale voluminoso. Quindi, l’assorbente si dissolve o si diffonde nella sostanza assorbente. Un ottimo esempio di questo fenomeno è un tovagliolo di carta che assorbe acqua e l’acqua alla fine si diffonde uniformemente su tutta la carta. Ci sono due modi in cui può avvenire l’assorbimento, attivo (trasporto attivo o diffusione facilitata) o passivo (diffusione). Inoltre, è un processo endotermico. Inoltre, il tasso di assorbimento dipende da molteplici fattori, tra cui la superficie esposta, la pressione e la concentrazione. Altri esempi di assorbimento includono:
- Acqua assorbita dai capelli
- L’anidride carbonica dall’aria viene assorbita dall’idrossido di sodio
- Ossigeno presente nell’atmosfera che si dissolve in acqua
- Cellule che assorbono nutrienti e acqua dall’ambiente circostante
Esempi di adsorbimento
Questo processo si verifica quando molecole, ioni o atomi aderiscono a una superficie. La sostanza adsorbita sulla superficie è chiamata adsorbente. Mentre l’adsorbente è la sostanza con la superficie. Poiché l’energia viene rilasciata quando l’adsorbato aderisce all’adsorbente, è considerato un processo esotermico. Pertanto, il tasso di adsorbimento dipende principalmente dalla temperatura e dalla superficie. Ad esempio, temperature più fredde promuovono l’adsorbimento a causa di particelle con minore energia termica aventi minore energia cinetica. Pertanto, è più probabile che aderiscano alle superfici a causa del legame idrogeno, della formazione di legami covalenti o di altre forze intermolecolari.
Esempi di adsorbimento includono:
- Contaminanti adsorbiti su carbone attivo
- L’argento si attacca al vetro e crea una superficie a specchio
- Acqua adsorbente su gel di silice
- Rivestimenti antiaderenti su pentole e padelle
- Particelle adsorbite su zeoliti
- Virus adsorbenti su superfici e cellule
- Refrigeratori ad adsorbimento utilizzati con refrigeranti
Usi: Assorbimento Vs. Adsorbimento
Assorbimento
Gli usi dell’assorbimento includono
- Idratazione
- Digestione
- Pulizia fuoriuscita
L’uso più comune dell’assorbimento è l’assorbimento per i refrigeratori per applicazioni di raffreddamento degli ambienti come celle frigorifere, raffreddamento dell’ingresso della turbina e produzione di ghiaccio. L’assorbimento è una scelta eccellente per i consumatori che cercano refrigeranti ecologici, funzionamento ad alta efficienza e combustibili a combustione pulita. Tuttavia, l’assorbimento di gas da parte del liquido viene utilizzato nella carbonatazione delle bevande e nell’idrogenazione degli oli.
Adsorbimento
Gli usi dell’adsorbimento includono acqua di raffreddamento per condizionatori d’aria, purificazione dell’acqua, trattamenti superficiali, colonne a scambio ionico e catalizzatori eterogenei. Pertanto alcune delle applicazioni industriali dell’adsorbimento includono:
- Refrigeratori ad adsorbimento
- Aria condizionata
- Purificazione dell’acqua
- Resina sintetica
I refrigeratori ad adsorbimento sono silenziosi perché non richiedono parti in movimento. Tuttavia, nelle applicazioni dell’industria farmaceutica, questo processo viene utilizzato come mezzo per estendere l’esposizione neurologica a determinati farmaci. Pertanto, l’adsorbimento di molecole su superfici polimeriche si verifica in diverse applicazioni come dispositivi biomedici e rivestimenti antiaderenti.
Il carbone attivo è assorbimento o adsorbimento?
Il carbone attivo è altamente poroso e ha una composizione chimica superficiale variabile. Pertanto, viene utilizzato nell’adsorbimento. Inoltre, fornisce un’ampia superficie per l’assorbimento dei contaminanti.
La cromatografia è assorbimento o adsorbimento del carbonio?
Le tecniche cromatografiche dipendono da quattro meccanismi di assorbimento, vale a dire partizione, esclusione dimensionale, adsorbimento superficiale e scambio ionico. Pertanto, il carbonio cromatografico è l’adsorbimento che coinvolge le molecole di soluto collegate direttamente alla superficie della fase stazionaria.
L’assorbimento e l’adsorbimento possono avvenire insieme?
Assorbimento contro adsorbimento, possono avvenire contemporaneamente? Si Loro possono. Quando questi due processi avvengono contemporaneamente, si parla di assorbimento. Ad esempio, quando qualcuno immerge una spugna nell’acqua, le molecole formano una pellicola sullo strato della spugna e, con il passare del tempo, si estende all’interno della massa della spugna.
<h3
Categoria: Articles